의료기기 정의
-
제조자가 다음과 같은 목적으로 인간을 위해 단독으로 또는 조합하여 사용하도록 의도한 기구, 장치, 도구, 기계, 기기, 임플란트, 체외 시약 또는 교정기, 소프트웨어, 재료 또는 기타 유사한 또는 관련 물품
- 1질병의 진단, 예방, 감시, 치료 또는 완화
- 2상해의 진단, 감시, 치료, 완화 또는 보조
- 3해부학이나 생리학적인 검사, 대체, 보정 또는 지원
- 4생명 유지
- 5임신 조절
- 6의료기기의 살균 소독
- 7의료정보를 제공하거나 인체에서 나온 검체의 체외 검사에 의한 진단
- 약리학적, 면역학적 또는 대사적 수단에 의해 인체 또는 인체 내에 대한 일차적인 의도된 작용을 달성하지 않지만, 그러한 수단에 의해 의도된 기능에 도움을 주는 것
등급 분류
- 의료기기(General): 의료기기 분류기준에 따라 Rule 1~16에 의해 분류
- 체외진단기기(IVDs): 개인 위험 및 공중 보건 위험 수준을 기반으로 Rule 1~7에 의해 분류
절차
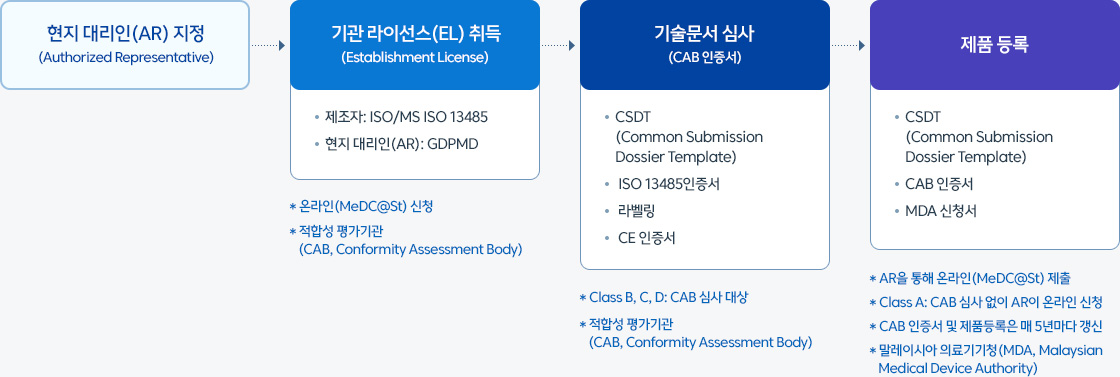
절차
- 현지 대리인(AR) 지정(Authorized Representative)
-
기관 라이선스(EL) 취득(Establishment License)
- 제조자: ISO/MS ISO 13485
- 현지 대리인(AR): GDPMD
* 온라인(MeDC@St) 신청
* 적합성 평가기관(CAB, Conformity Assessment Body)
-
기술문서 심사(CAB 인증서)
- CSDT(Common Submission Dossier Template)
- ISO 13485인증서
- 라벨링
- CE 인증서
* Class B, C, D: CAB 심사 대상
* 적합성 평가기관(CAB, Conformity Assessment Body)
-
제품 등록
- CSDT(Common Submission Dossier Template)
- CAB 인증서
- MDA 신청서
* AR을 통해 온라인(MeDC@St) 제출
* Class A: CAB 심사 없이 AR이 온라인 신청
* CAB 인증서 및 제품등록은 매 5년마다 갱신
* 말레이시아 의료기기청(MDA, Malaysian Medical Device Authority)
출처
- Guidance Document - Medical Device Authority (MDA)
- MDA-GD-0006 Definition of Medical Device
- MDA-GD-0009 Rules of Classification for General Medical Devices
- MDA-GD-0001 In-Vitro Diagnostics (IVD) Medical Device Classification
- MDA-GD-0031 Conformity Assessment for Medical Device

